

基礎研究
もやもや病の発症素因遺伝子と病態修飾因子の解明
私たち北海道大学脳神経外科では、もやもや病の疾患概念が確立する頃から、 原因の探索・診断法・治療法の確立を目指して診療・研究を続けてきました。 特に日本人や韓国人など東アジア人におけるもやもや病発症の背景には、 17番染色体長腕に位置するもやもや病の疾患感受性遺伝子RNF213の変異が色濃く関わっているという、 世界的に見ても画期的な発見があり、現在は10年が経過したところです。 長年にわたるもやもや病の患者さんの診療経験をもとに、研究の趣旨にご賛同いただける患者さんやご家族のご協力を得ながら、 臨床的情報を体系的に収集記録分析し、血液をはじめとする生体試料から、 遺伝子ゲノム情報、遺伝子配列によらないエピゲノム情報、タンパク質発現の情報解析を推進しています。 これにより、もやもや病の発症素因遺伝子と病態修飾因子を解明して、病気の根本的な治療開発を目指しています。(2021年7月)
Genotyping assay (real-time PCR)
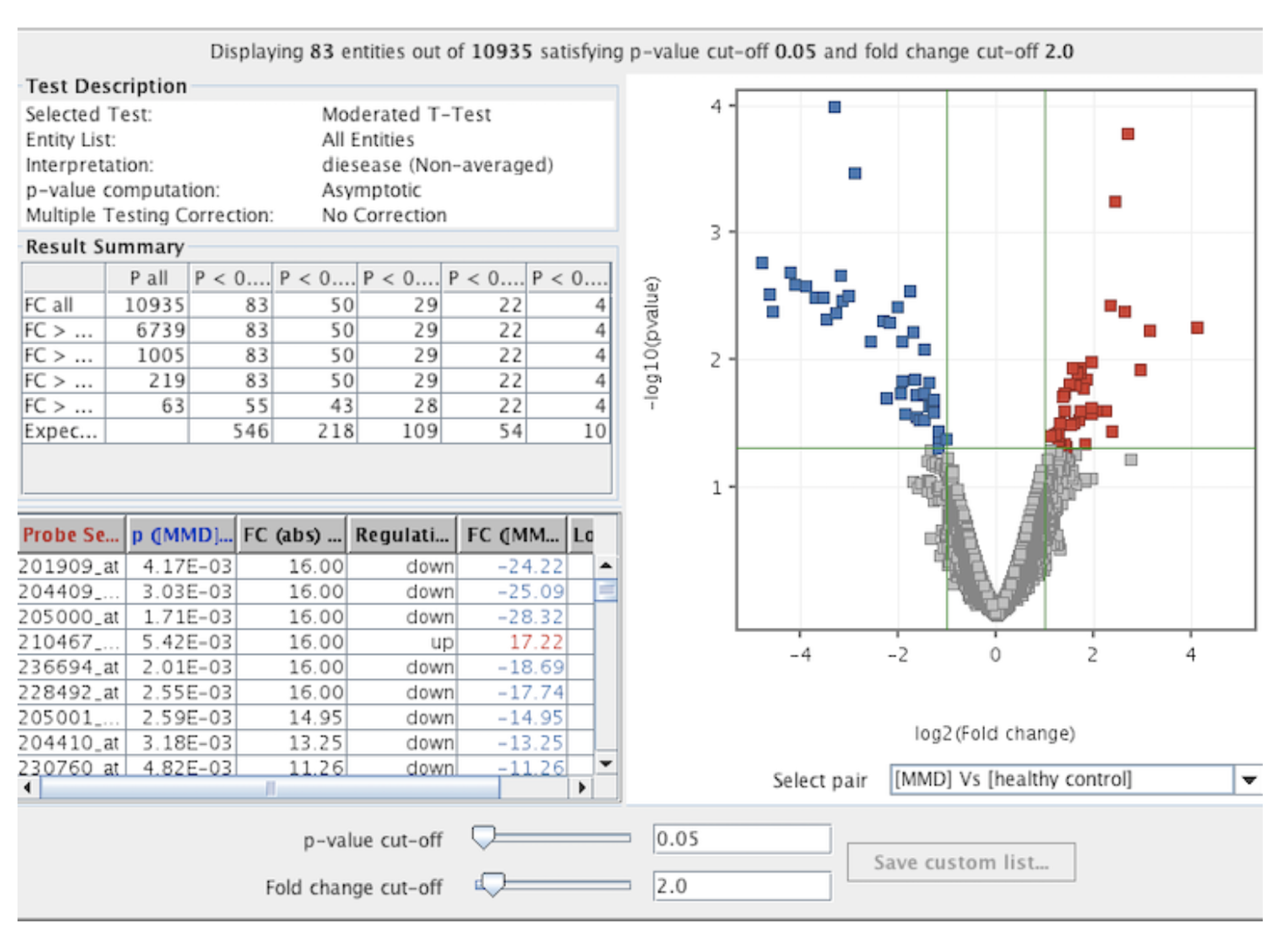
Differential gene expression analysis

Transcriptome assay (microarray)
もやもや病iPS由来細胞を用いた病態発生メカニズムの解明
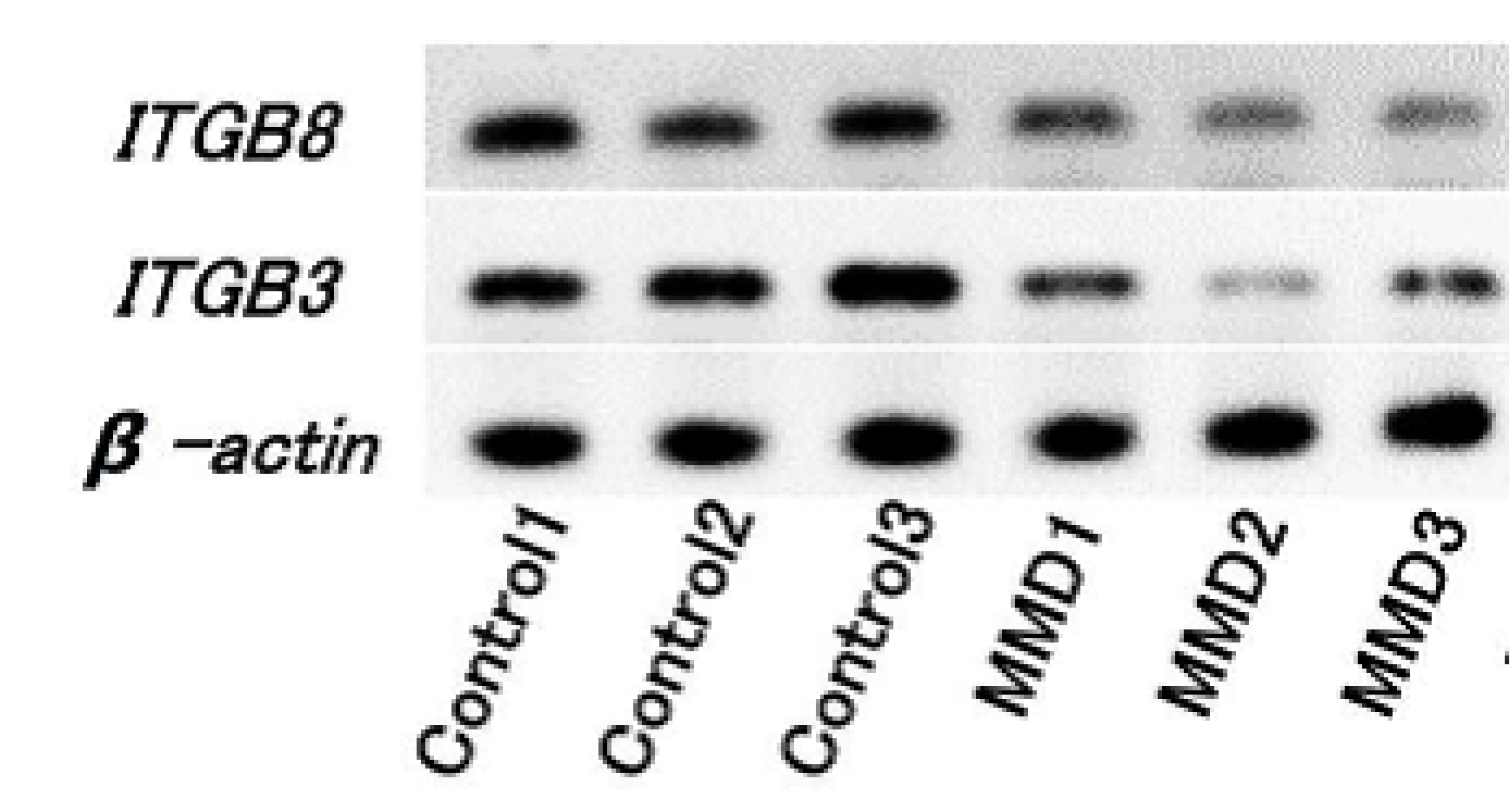
RNF213遺伝子はもやもや病の疾患関連遺伝子として近年注目されています。 我々はこの遺伝子変異を持つもやもや病患者の末梢血単核球よりiPS細胞を樹立することに成功しました。 このiPS細胞より分化誘導した血管内皮細胞において、接着分子インテグリンの発現が低下していました(図参照)。 今後、このiPS由来血管内皮細胞を用いて、インテグリン機能に関わる細胞接着、シェアストレス応答等の変化を検討していく予定です。 また血管平滑筋細胞を誘導することも試みており、これらの検討から、もやもや病の病態発生メカニズムを解明したいと考えています。
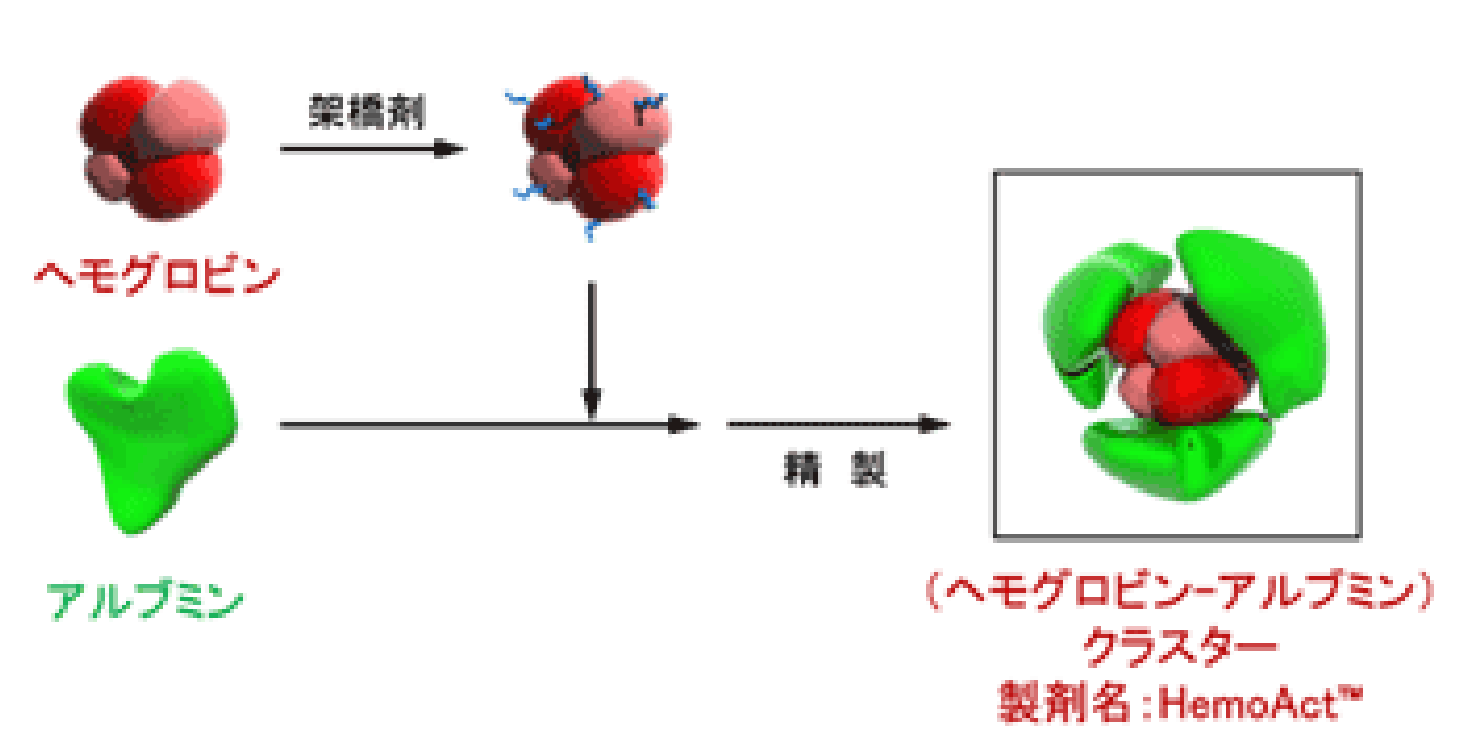
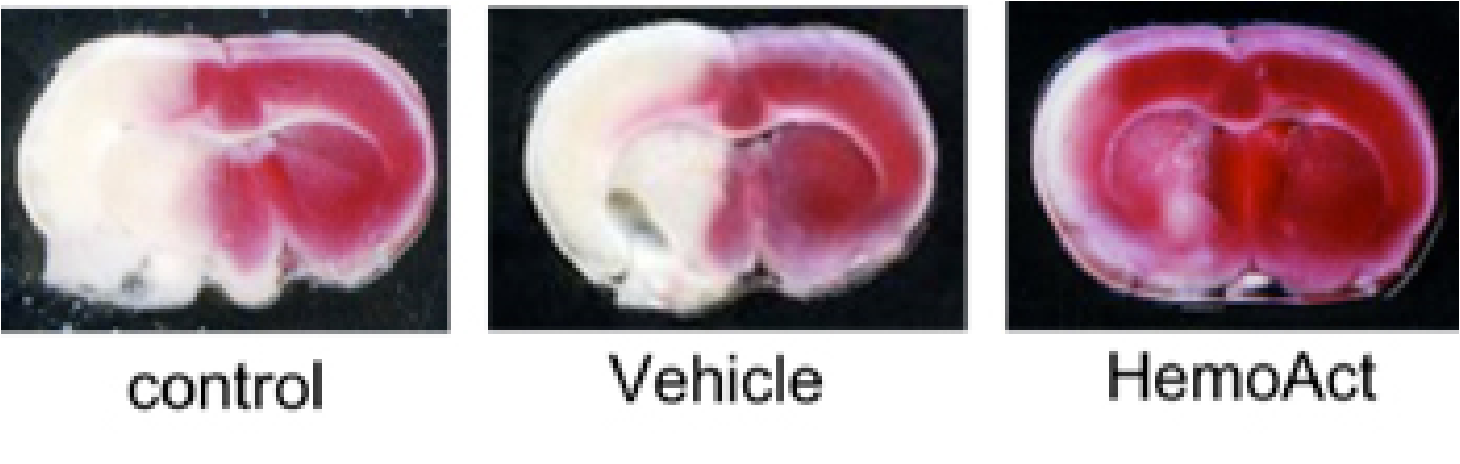
人工酸素運搬体による急性期脳虚血に対する脳保護療法
人工酸素運搬体は一般に粒径が赤血球より小さいことから、 微小血管において良好に灌流し、脳虚血時には有効に作用するものと考えられます。 近年、臨床応用の可能性が高い人工酸素運搬体として蛋白質クラスター型のヘモグロビン製剤であるHemoAct(図参照)が 注目を集めています。我々はこのHemoActを用いて、急性期脳虚血における脳保護効果を検討しています (製剤開発した中央大学理工学部 小松研究室との共同研究)。 ラットの一過性中大脳動脈閉塞モデルの検討では、HemoActを投与することにより、 梗塞縮小効果(図参照)と微小血管での良好な灌流を認めました。 今後、種々な脳虚血条件下での治療効果の検討をしていく予定でいます。
脳や脊髄の病気に対する骨髄間質細胞再生治療の開発
脳や脊髄の病気では、しばしば重篤な後遺症が生じます。 たくさんの新規治療法が開発されつつありますが、 中枢神経系では再生能力が限定的であるため、その治療効果は不十分です。 近年、再生医療研究が急速に進歩しており、中枢神経疾患に対する骨髄間質細胞移植治療が期待されています。 我々は脳梗塞・脳出血・脊髄損傷・認知症などの動物モデルを用いて、 幹細胞・幹細胞足場材複合体・幹細胞分泌物(エクソソーム)などを用いて、 機能回復が得られないかどうかの研究を進めています。また研究の実用化に向けて、 自動培養装置の開発や知的財産権(特許)の取得などにも着手しております。
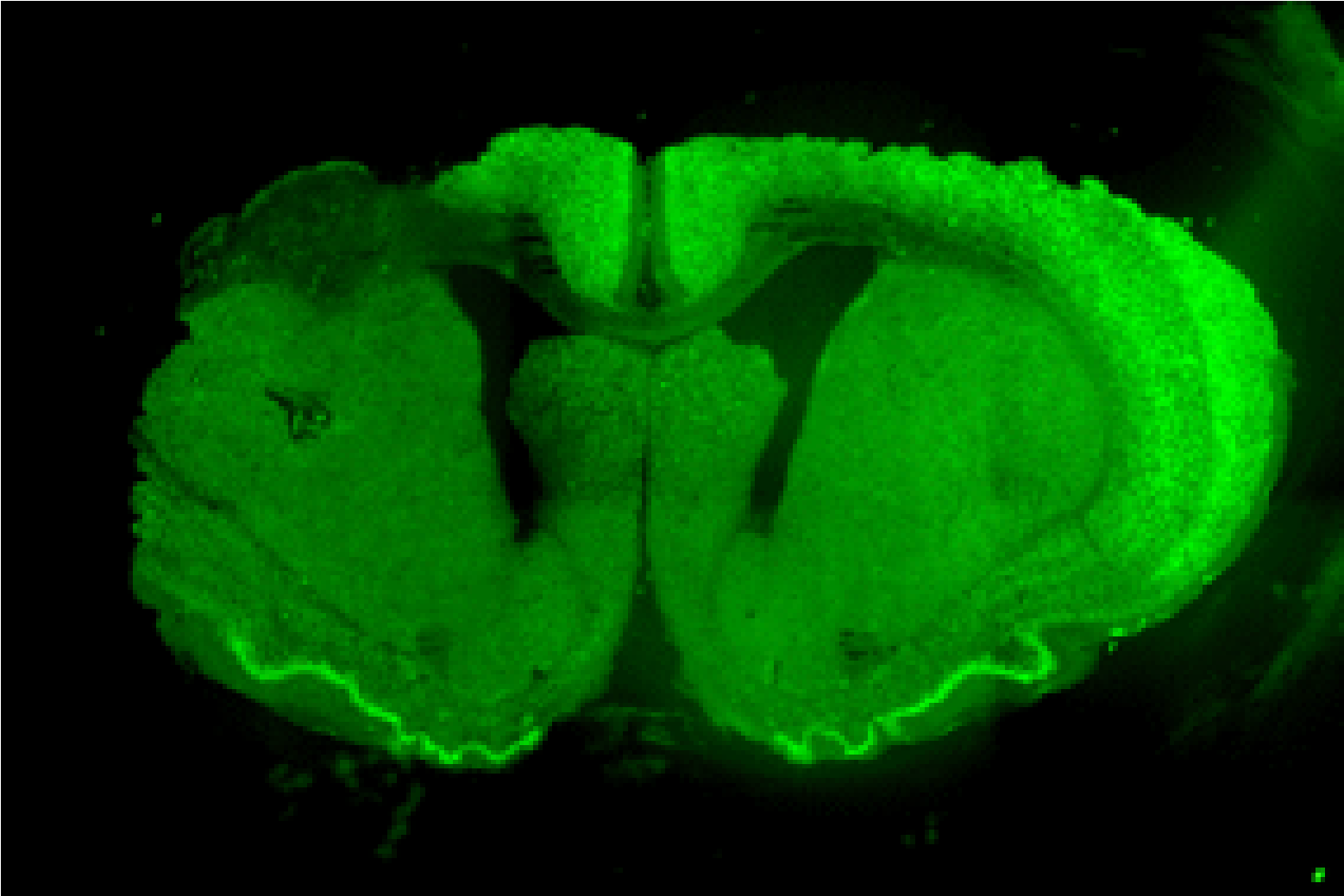
動物モデルで幹細胞の効果を確認しています
培養された幹細胞
脊髄疾患に対する間葉系幹細胞シート移植の研究
重篤な脊髄疾患は、四肢麻痺・感覚障害や膀胱直腸障害等を後遺し、日常生活を著しく妨げることも稀ではありません。
しかし、不可逆的となった神経損傷に対しては、有効な治療は依然として少ないため、再生医療の臨床応用などの新しい治療の発展が期待されています。脊髄グループでは、幹細胞移植を用いた脊髄疾患治療の開発を目指し、様々な動物実験による検証を積み重ねています。
ラット脊髄損傷亜急性期モデルに対する同種骨髄間葉系幹細胞から作成した幹細胞シート脊髄損傷部硬膜下移植の検討では、同数の脊髄髄内直接細胞注射と比べても運動・感覚機能の良好な治療成績が認められており、その作用メカニズムの解明と今後の臨床応用へ向けてのデータを蓄積しています。
さらに、ラット脊髄髄膜瘤モデルを用いて羊水幹細胞シート移植による胎児手術の開発を目指した研究も開始しており、脊髄疾患の治療発展への貢献を目指し、研究を続けています。

培養中の細胞シート
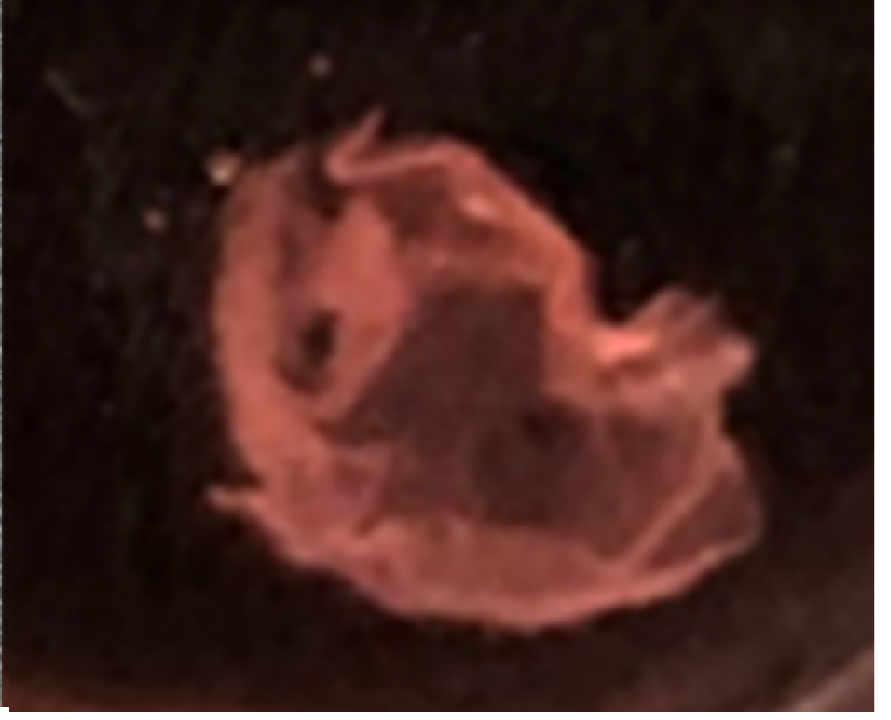
剥離後の細胞シート
ラット脊髄損傷部硬膜下への細胞シート移植
脳腫瘍のPET所見の分子生物学的検証
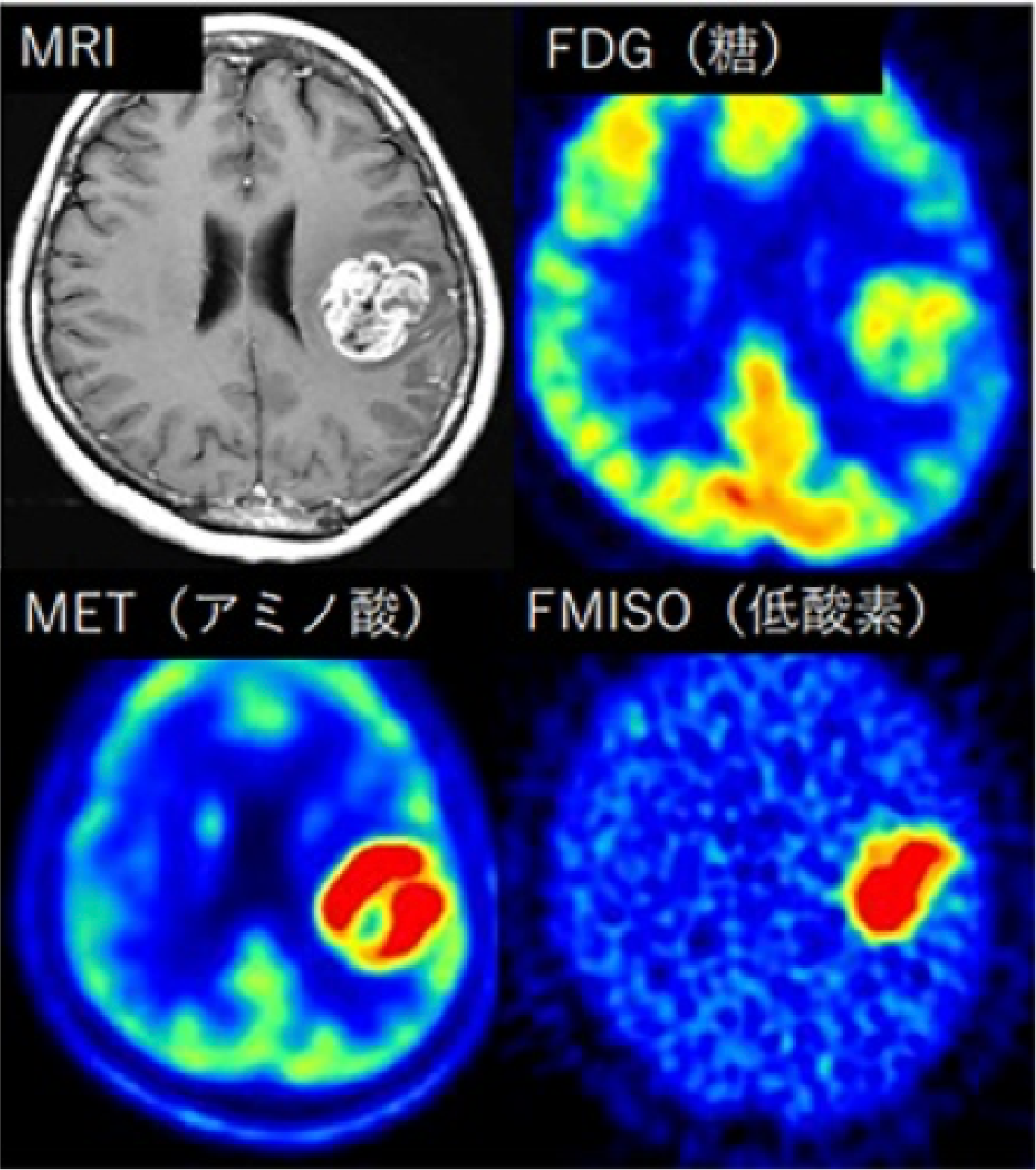
脳腫瘍診断はMRIを用いて行うことが一般的ですが、 当院では代謝イメージングであるPET(ポジトロン断層撮影法)を積極的に併用しています(図)。 腫瘍内の糖代謝、アミノ酸代謝、低酸素状態等を可視化できる診断方法ですが、 基礎研究ではこれらの診断で得られた情報と、手術で得られた腫瘍検体を組み合わせて分子生物学的な解析を行っています。 この研究から、予後予測につながる分子マーカーの発見、治療標的分子、腫瘍代謝メカニズムなどの解明を目指しています。
遺伝子情報に基づいた脳腫瘍の分子分類と臨床情報の統合解析
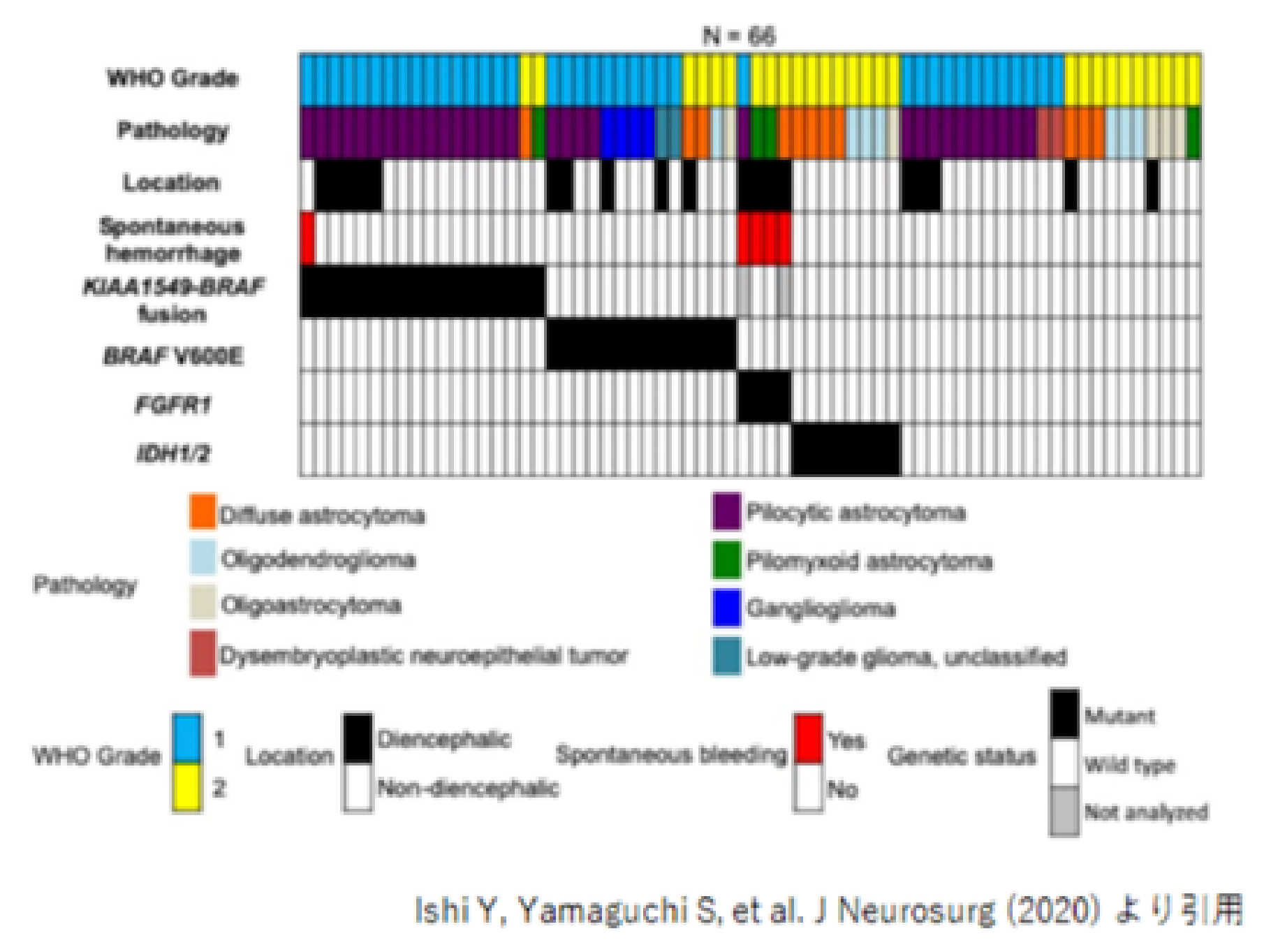
近年様々な脳腫瘍の遺伝子解析が進み、 多くの腫瘍発生原因となる遺伝子異常が発見されてきています。 当教室では、患者さんから摘出した脳腫瘍を凍結検体として多数保存してきました。 この保存検体を使用して遺伝子解析を行い、分子分類として新たな枠組みを構築し、 さらに詳細な臨床情報と合わせて解析することで、新たな知見の発見を目指しています。 神経膠腫、中枢神経原発リンパ腫、髄膜腫などの腫瘍に関して、検証を進めています。 図は小児脳腫瘍の一種である毛様細胞性星細胞腫と遺伝子異常、 臨床症状の関連性の報告からの抜粋です。
ソフトマターを用いた新たな塞栓物質の開発
脳血管内治療は使用する道具が進歩することにより、 その治療を根本的に変える可能性が期待される領域です。 我々はソフトマターテクノロジーを用いて (北海道大学 先端生命科学研究院 ソフト&ウェットマター研究室 黒川孝幸先生との共同研究)、 新たな塞栓物質に取り組んでいます(図参照)。 塞栓物質は脳腫瘍などの異常血管を閉塞するための物質ですが、 これまでの塞栓物質はレントゲンで見えないため、造影剤などを混ぜて注入していました。 もし塞栓物質自体がレントゲンで見えると効果的かつ安全に治療ができることが期待されます。 この研究により、レントゲンで見える塞栓物質が開発できれば、 血管塞栓術の新たな世界が開けると考えられます。



